내용요약
허가일부터 7년간 시장독점 기간 보장
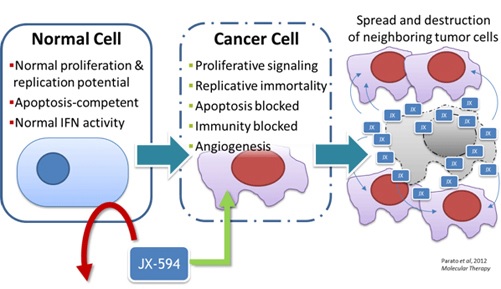
[한스경제=이상빈 기자] 신라젠의 면역 항암제 후보물질 '펙사벡'이 미국 식품의약국(FDA)으로부터 IIB-IV단계(2기) 흑색종 치료용 희귀의약품 지정을 승인받았다고 27일 밝혔다.
신라젠은 허가일로부터 7년 동안 시장 독점 기간을 보장받고, 미국 내 임상시험 비용 50% 세금 감면과 허가심사 기간 단축 등의 자격을 얻는다.
흑색종은 피부암으로 불리며 멜라닌세포가 존재하는 부위 어디서든 발병한다. 피부암 중 악성도가 높지만 자각 증상이 없고 평범한 점 또는 결절(1cm 이상 크기의 솟아오른 피부병변)로 보인다.
펙사벡이 희귀의약품으로 지정된 적응증(치료범위)은 IIB-IV 단계인 고위험군의 흑색종이다. IIB는 종양의 두께가 2.01~4밀리미터(mm)로 궤양이 있는 상태 또는 종양의 두께가 4.01mm 이상의 상태를 의미한다.
IIB-IV 단계에서 치료하지 못하면 림프절 전이가 확대될 수 있고, 림프절 침범이 발생하면 5년 생존율이 30% 수준으로 떨어진다.
신라젠 관계자는 "개발 단계에서 희귀의약품으로 지정된 건 의료적 중요성, 안전성, 가능성을 높게 판단한 결과"라며 "펙사벡이 희귀의약품 지정을 발판 삼아 현재 진행하는 다양한 임상시험에서 긍정적인 결과를 도출하도록 노력하겠다"고 설명했다.
이상빈 기자 pkd@sporbiz.co.kr
이상빈 기자
pkd@sporbiz.co.kr


