유플라이마, 2분기 유럽 출시 가능성

[한스경제=변동진 기자] 셀트리온그룹의 신제품 ‘램시마SC’와 ‘유플라이마’가 올 초부터 본격적인 유럽 시장 공략을 시작했다.
셀트리온헬스케어에 따르면 램시마SC는 유럽 5국가 중 독일, 영국, 프랑스 등에 이어 최근 스페인과 이탈리아에 각각 출시됐다. 이들 국가는 유럽 시장의 70%를 차지하는 주요 국가다. 비슷한 시기 벨기에, 포르투갈, 핀란드 등에서 론칭했다.
램시마SC는 레미케이드 바이오시밀러 ‘램시마’를 정맥주사(IV) 제형에서 피하주사(SC) 제형으로 개량한 품목이다. 환자가 복부나 허벅지 등에 직접 주사기로 약물을 주입할 수 있다는 장점이 있다.
유럽뿐 아니라 북미 시장 진출을 위한 작업도 순항 중이다. 램시마SC는 지난 1월 말 류머티즘 관절염 적응증으로 캐나다 보건부(Health Canada)로부터 판매 승인을 획득했다.
셀트리온헬스케어는 현지 법인을 설립해 램시마SC를 직접 판매하고, 향후 ‘염증성 장질환(IBD)’에 대해서도 허가 신청할 계획이다. 미국에서는 임상 3상을 진행하고 있다.
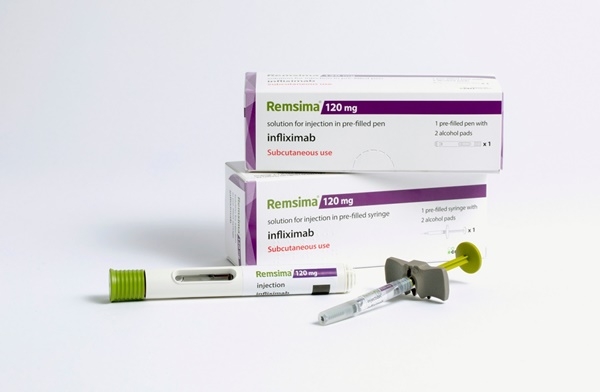
이와 함께 고농도 휴미라 바이오시밀러(복제약) ‘유플라이마’는 이르면 2분기 중 독일 등 주요 유럽 국가에 출시될 수 있다.
유럽연합 집행위원회(EC)는 지난 2월 유플라이마 판매를 허가했다. 현재 류마티스 관절염과 염증성 장질환, 건선 등 오리지널 품목이 보유한 모든 적응증에 대해 사용할 수 있다.
유플라이마의 특징은 ‘고농도’라는 점이다. 회사는 주사 시 통증을 유발할 수 있는 시트르산염(구연산염)을 제거, 통증을 줄였다. 구연산염이 제거되면서 주성분이 똑같은 양으로 들어가도 주사액 용량은 절반으로 줄어든다. 때문에 ‘CF(Citrate Free)’ 제형 또는 고농도로 불린다. 현재 유럽에서 판매되는 휴미라의 90% 이상은 CF 제형인 것으로 알려졌다.
셀트리온헬스케어는 세계 최초 고농도 휴미라 바이오시밀러라는 점을 적극 활용해 유플라이마의 유럽 시장 점유율을 빠르게 확대할 방침이다.
한편 셀트리온헬스케어 관계자는 램시마SC와 관련해 “독일, 영국, 프랑스, 이탈리아 등 유럽 주요 5개국 외에 출시를 목표한 모든 국가에서 제품을 론칭했다”면서 “다만 연간 예상(목표) 매출은 투자자에 영향을 줄 수 있기 때문에 현재 밝힐 수 있는 단계는 아니다”고 말했다.
변동진 기자 bdj@sporbiz.co.kr


