희귀의약품 지정 시 세금 감면 등 각종 혜택
[한스경제=김지영 기자] 세계 최대 의약품 시장인 미국에서 국내 제약·바이오기업이 개발 중인 신약 후보 물질이 희귀의약품 지정을 받아 눈길을 끈다.
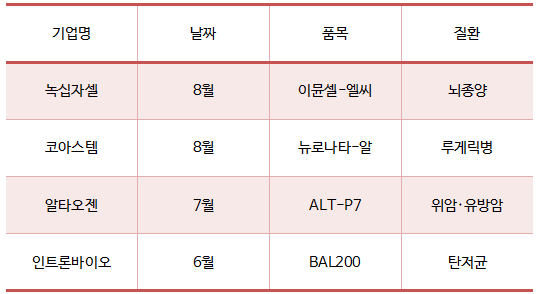
4일 업계에 따르면 올해 FDA로부터 희귀의약품 지정을 받은 업체는 녹십자셀, 코아스템, 알타오젠, 인트론바이오다.
희귀의약품 지정은 난치병과 같은 생명을 위협하는 질병 치료제 연구 개발이 원활하게 이뤄질 수 있도록 개발 업체에 다양한 혜택을 부여하는 제도다. 희귀의약품으로 지정되면 △세금 감면 혜택 △신약 승인 심사 비용 면제 △시판 허가 승인 후 7년간 독점권 인정 등의 헤택을 받을 수 있다.
글로벌 제약산업 분석업체 이벨류에이트파마에 따르면 세계 희귀의약품 시장규모는 2013년 약 100조원에서 2020년 196조원으로 성장할 전망이다. 전세계 전문의약품 가운데 희귀의약품이 차지하는 비중도 지난해 13.9%에서 2020년 18%에 이를 것으로 보인다. FDA를 비롯, 유럽 의약품감독국(EMA) 등 선진국들이 희귀의약품 개발을 독려하기 위해 관련 규제 완화 및 각종 혜택을 제공하며 관련 시장은 더 커질 것으로 예상된다.
가장 최근 희귀의약품을 지정받은 업체는 녹십자셀이다. 녹십자셀은 지난 8월17일 뇌종양(교모세포종)을 대상으로 항암 면역세포치료제 이뮨셀-엘씨에 대한 희귀의약품 지정을 승인받았다. 이뮨셀-엘씨는 환자의 혈액을 원료로 만드는 환자 개인별 맞춤 항암제다.
녹십자셀은 췌장암에 대한 희귀의약품 지정도 추가로 신청하고 결과를 기다리고 있다. 녹십자셀 관계자는 “췌장암 치료제의 경우 올해 안에 희귀의약품 지정 결과가 나올 것으로 보인다”고 말했다.
바이오업체 코아스템은 루게릭병 줄기세포 치료제 ‘뉴로나타-알’이 지난 8월4일 희귀의약품으로 지정됐다. 뉴로나타-알은 2014년 12월 임상 2상 후 조건부 시판허가를 받아 2015년 국내 시판된 바 있다.
또 다른 바이오업체 알타오젠은 유방암치료제 ‘허셉틴’을 이용한 위암치료제 희귀의약품 등록을 마쳤다. 이 치료제는 지난해 국내 식품의약품안전처 승인을 받아 유방암 환자를 대상으로 임상 1상을 진행하고 있다.
인트론바이오도 탄저균 감염 치료제로 개발 중인 ‘N-RephasinBAL200’가 올해 FDA 희귀의약품으로 지정됐다.
업계 관계자는 “희귀의약품은 절대 환자 수는 적지만 미국에서 개발을 장려하며 시장이 점차 확대되고 있다”며 “만성질환 지료제보다 데이터를 확보하기 쉽기 때문에 희귀의약품 개발에 대한 제약사들의 관심이 높아지고 있다”고 말했다.
김지영 기자 jiyoung91@sporbiz.co.kr


